药物/医疗器械临床试验质量管理规范培训
——暨临床试验技能提高培训班
(第一轮通知)
中国.南昌
各药物临床试验机构、临床试验伦理委员会及相关单位:
为紧跟我国临床试验质量管理规范的发展步伐,帮助研究单位及医疗机构以及临床研究人员更好的理解和掌握临床试验相关法规和临床试验操作的技巧。解答在开展临床试验时遇到诸多技术层面的实际问题,进一步提升对药物临床试验的质量与安全的掌控能力,科学、严谨地组织好临床试验的研究工作,切实提高科研能力和管理水平,更好的为“人民用药安全”这一目标服务。为此,拟于2019年12月10日在江西省南昌市举办“药物/医疗器械临床试验质量管理规范培训班”。本次培训将邀请我国临床试验相关领域的资深专家,围绕例如:新药品管理法对临床试验的影响、药物临床试验科学设计与可操作性之间关键要素、创新药物的伦理审查等内容给予学员们现场指导,并为大家解惑和讨论临床工作中遇到的实际问题。本次培训由中国药理学会药物临床试验专业委员会主办,江西省药物临床试验与研究学会与南昌大学第一附属医院联合承办。
一、参会对象
1、医疗机构临床试验机构及伦理委员会的成员;
2、 医疗机构从事临床试验的医生、护士及相关人员;
3、制药企业的药物临床研究部门、质量管理部门的团队成员;
4、CRO公司、SMO公司、高校及科研院所等单位的项目团队成员。
二、日程安排
1、报到时间:
2019年12月10日(07:30~08:30)
2、报到酒店:
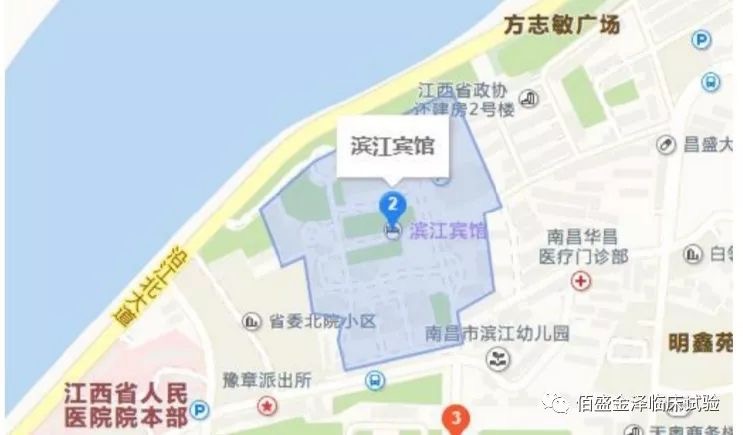
滨江宾馆(南昌市东湖区爱国路216号)
3、报到时间:
2019年12月09日(15:00-21:00) 11号楼 大厅
2019年12月10日(07:30-08:30)大会堂 一楼
4、培训时间:2019年12月10日 全天
5、培训地点:大会堂 一楼 多功能厅
三、培训地址
1、会议地点:
南昌滨江宾馆(电话:0791-88822168)
2、会议地址:
南昌市东湖区爱国路216号;距离南昌西站18公里,距离昌北机场31公里。
3、注意事项:请所有参会代表自行预订住宿,费用自理,由于近期会务较多导致住宿紧张,请务必提前做好酒店预订。会务组统一安排12月10日当天的中餐。
四、培训内容
1、临床试验法规与技术规范的进展及对临床试验的影响
2、迎接挑战,如何做好创新药的伦理审查
3、医疗器械临床试验与药物临床试验异同内容的比较
4、医疗器械及诊断试剂临床试验的规范化要素
5、药物临床试验安全性事件的管理
6、多中心临床试验项目数据核查的要点及案例分析
五、培训证书
参加全程学习并通过结业考试的学员将获得“药物/医疗器械临床试验质量管理规范培训暨临床试验技能提高培训班”证书。
六、培训报名及费用
1、培训费用600元/人,学员的住宿、交通及其他餐饮费用自理;
2、银行汇款或现场报到时通过刷卡、支付宝转账或现金缴纳;
3、会务组在培训结束后10个工作日内寄送证书和“会务费(GCP培训)”发票;
4、培训报名截止时间:2019年12月8日
七、报名方式
请在报名回执(见附件)中填写好参加培训人员信息,填好回执后请发送到:
报名邮箱 E-mail:
中国药理学会药物临床试验专业委员会 会务筹备组:chinadctc@126.com ;
江西省药物临床试验与研究学会 会务筹备组:2829182620@qq.com;
南昌大学第一附属医院 会务筹备组:sunwenxionggcp@163.com
联系人:
中国药理学会药物临床试验专业委员会 会务组:李裕(13962165602)
南昌大学第一附属医院 国家药物临床试验机构:孙文雄(15170068525);白薇(13870689675)
江西省药物临床试验与研究学会 秘书处:刘雪梅(18702536007)
中国药理学会药物临床试验专业委员会
江西省药物临床试验与研究学会
南昌大学第一附属医院国家药物临床试验机构
2019年11月25日
附件:
药物/医疗器械临床试验质量管理规范培训
——暨临床试验技能提高班(南昌)
报名回执
|
联系人 |
手机 |
||||
|
单位名称 |
联系电话 |
||||
|
通讯地址 |
|||||
|
缴费方式 |
□现金 □刷卡 □汇款 |
||||
|
发票类型 |
□增值税普通发票 □增值税专用发票 |
||||
|
增值税专用发票信息 |
开票单位名称 |
||||
|
纳税人识别号 |
|||||
|
地址及电话 |
|||||
|
开户行及账号 |
|||||
|
姓名 |
性别 |
职务/职称 |
手机号码 |
E-mail地址 |
|
备注:培训报名截止时间:2019年12月8日



 微信
微信

 高级网站搜索
高级网站搜索